ఎలక్ట్రోలైట్ అంటే ఏమిటి
అయాన్ల కదలిక కారణంగా విద్యుత్ ప్రవాహం ఏర్పడే పదార్థాలు, అనగా. అయానిక్ వాహకతఎలక్ట్రోలైట్స్ అంటారు. ఎలక్ట్రోలైట్లు రెండవ రకానికి చెందిన కండక్టర్లకు చెందినవి, ఎందుకంటే వాటిలోని విద్యుత్తు రసాయన ప్రక్రియలకు సంబంధించినది, మరియు కేవలం లోహాలలో వలె ఎలక్ట్రాన్ల కదలికకు సంబంధించినది కాదు.
ద్రావణంలో ఉన్న ఈ పదార్ధాల అణువులు విద్యుద్విశ్లేషణ విచ్ఛేదనం చేయగలవు, అనగా, ధనాత్మకంగా చార్జ్ చేయబడిన (కాటయాన్స్) మరియు ప్రతికూలంగా చార్జ్ చేయబడిన (అయాన్లు) అయాన్లుగా కరిగిపోయినప్పుడు అవి కుళ్ళిపోతాయి. ఘన ఎలక్ట్రోలైట్లు, అయానిక్ కరుగుతుంది మరియు ఎలక్ట్రోలైట్ పరిష్కారాలు ప్రకృతిలో కనిపిస్తాయి. ద్రావకం యొక్క రకాన్ని బట్టి, ఎలక్ట్రోలైట్లు సజల మరియు నాన్-సజల, అలాగే ఒక ప్రత్యేక రకం - పాలిఎలెక్ట్రోలైట్స్.
నీటిలో కరిగినప్పుడు పదార్ధం కుళ్ళిపోయే అయాన్ల రకాన్ని బట్టి, H + మరియు OH- అయాన్లు లేని ఎలక్ట్రోలైట్లు (ఉప్పు ఎలక్ట్రోలైట్లు), H + అయాన్లు (యాసిడ్లు) సమృద్ధిగా ఉన్న ఎలక్ట్రోలైట్లు మరియు OH- అయాన్ల ప్రాబల్యం ఉన్న ఎలక్ట్రోలైట్లు ( బేస్) వేరు చేయవచ్చు.
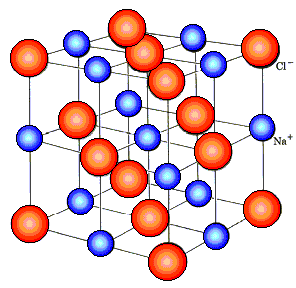
ఎలక్ట్రోలైట్ అణువుల విచ్ఛేదనం సమయంలో సమాన సంఖ్యలో సానుకూల మరియు ప్రతికూల అయాన్లు ఏర్పడినట్లయితే, అటువంటి ఎలక్ట్రోలైట్ను సిమెట్రిక్ అంటారు.లేదా ద్రావణంలో సానుకూల మరియు ప్రతికూల అయాన్ల సంఖ్య ఒకేలా లేకుంటే అసమానంగా ఉంటుంది. సిమెట్రిక్ ఎలక్ట్రోలైట్స్ ఉదాహరణలు - KCl - 1,1-వాలెంట్ ఎలక్ట్రోలైట్ మరియు CaSO4 - 2,2-వాలెంట్ ఎలక్ట్రోలైట్. అసమాన ఎలక్ట్రోలైట్ యొక్క ప్రతినిధి, ఉదాహరణకు, H2TAKA4 — 1,2-వాలెంట్ ఎలక్ట్రోలైట్.

అన్ని ఎలక్ట్రోలైట్లను వాటి విడదీయగల సామర్థ్యాన్ని బట్టి స్థూలంగా బలమైన మరియు బలహీనంగా విభజించవచ్చు. పలుచన ద్రావణాలలో బలమైన ఎలక్ట్రోలైట్లు దాదాపు పూర్తిగా అయాన్లుగా కుళ్ళిపోతాయి. వీటిలో పెద్ద సంఖ్యలో అకర్బన లవణాలు, సజల ద్రావణాలలో కొన్ని ఆమ్లాలు మరియు స్థావరాలు లేదా ఆల్కహాల్లు, కీటోన్లు లేదా అమైడ్లు వంటి అధిక విచ్ఛేదన శక్తి కలిగిన ద్రావకాలు ఉన్నాయి.
బలహీనమైన ఎలక్ట్రోలైట్లు పాక్షికంగా మాత్రమే కుళ్ళిపోతాయి మరియు అవి విడదీయబడని అణువులతో డైనమిక్ సమతుల్యతలో ఉంటాయి. వీటిలో పెద్ద సంఖ్యలో సేంద్రీయ ఆమ్లాలు అలాగే ద్రావకాలలో అనేక స్థావరాలు ఉన్నాయి.
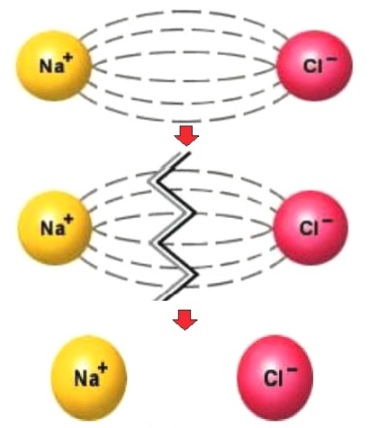
డిస్సోసియేషన్ డిగ్రీ అనేక అంశాలపై ఆధారపడి ఉంటుంది: ఉష్ణోగ్రత, ఏకాగ్రత మరియు ద్రావకం రకం. కాబట్టి, ఒకే విద్యుద్విశ్లేషణ వివిధ ఉష్ణోగ్రతల వద్ద, లేదా అదే ఉష్ణోగ్రత వద్ద కానీ వేర్వేరు ద్రావకాలలో, వివిధ డిగ్రీలకు విడదీయబడుతుంది.
విద్యుద్విశ్లేషణ విచ్ఛేదం, నిర్వచనం ప్రకారం, ద్రావణంలో పెద్ద సంఖ్యలో కణాలను ఉత్పత్తి చేస్తుంది కాబట్టి, ఇది ఎలక్ట్రోలైట్స్ మరియు వివిధ రకాల పదార్థాల యొక్క భౌతిక లక్షణాలలో గణనీయమైన వ్యత్యాసాలకు దారితీస్తుంది: ద్రవాభిసరణ పీడనం పెరుగుతుంది, ద్రావకం స్వచ్ఛతకు సంబంధించి ఘనీభవన ఉష్ణోగ్రత మారుతుంది. మరియు ఇతరులు.
ఎలక్ట్రోలైట్ అయాన్లు తరచుగా ఎలక్ట్రోకెమికల్ ప్రక్రియలు మరియు రసాయన ప్రతిచర్యలలో స్వతంత్ర గతి యూనిట్లుగా పాల్గొంటాయి, ద్రావణంలో ఉన్న ఇతర అయాన్ల నుండి స్వతంత్రంగా ఉంటాయి: ఎలక్ట్రోలైట్లో మునిగిపోయిన ఎలక్ట్రోడ్లపై, ఎలక్ట్రోలైట్ గుండా కరెంట్ వెళ్ళినప్పుడు, ఆక్సీకరణ-తగ్గింపు ప్రతిచర్యలు జరుగుతాయి. ఇవి ఎలక్ట్రోలైట్ కూర్పుకు జోడించబడతాయి.
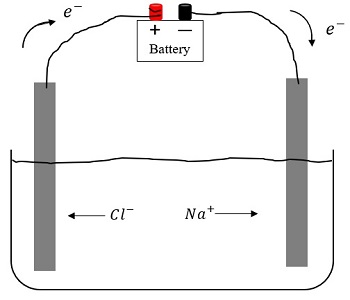
అందువల్ల, ఎలక్ట్రోలైట్లు అయాన్లు, ద్రావణి అణువులు, విడదీయబడని ద్రావణ అణువులు, అయాన్ జతలు మరియు పెద్ద సమ్మేళనాలను కలిగి ఉన్న పదార్ధాల సంక్లిష్ట వ్యవస్థలు. అందువల్ల, ఎలక్ట్రోలైట్స్ యొక్క లక్షణాలు అనేక కారకాలచే నిర్ణయించబడతాయి: అయాన్-మాలిక్యులర్ మరియు అయాన్-అయాన్ పరస్పర చర్యల స్వభావం, కరిగిన కణాల సమక్షంలో ద్రావకం యొక్క నిర్మాణంలో మార్పులు మొదలైనవి.
పోలార్ ఎలక్ట్రోలైట్స్ యొక్క అయాన్లు మరియు అణువులు ఒకదానితో ఒకటి చాలా చురుకుగా సంకర్షణ చెందుతాయి, ఇది సాల్వేషన్ నిర్మాణాల ఏర్పాటుకు దారితీస్తుంది, అయాన్ల పరిమాణం తగ్గడం మరియు వాటి విలువల పెరుగుదలతో పాత్ర మరింత ముఖ్యమైనది. సాల్వేషన్ ఎనర్జీ అనేది ద్రావణి అణువులతో ఎలక్ట్రోలైట్ అయాన్ల పరస్పర చర్య యొక్క కొలత.
ఎలెక్ట్రోలైట్స్, వాటి ఏకాగ్రతపై ఆధారపడి ఉంటాయి: పలుచన పరిష్కారాలు, తాత్కాలిక మరియు కేంద్రీకృతమై ఉంటాయి. పలుచన ద్రావణాలు నిర్మాణంలో స్వచ్ఛమైన ద్రావకం వలె ఉంటాయి, అయితే ప్రస్తుతం ఉన్న అయాన్లు వాటి ప్రభావంతో ఈ నిర్మాణాన్ని భంగపరుస్తాయి. అయాన్ల మధ్య ఎలెక్ట్రోస్టాటిక్ ఇంటరాక్షన్ కారణంగా బలమైన ఎలక్ట్రోలైట్ల యొక్క ఇటువంటి బలహీనమైన పరిష్కారాలు లక్షణాలలో ఆదర్శ పరిష్కారాల నుండి భిన్నంగా ఉంటాయి.
ఏకాగ్రత యొక్క పరివర్తన ప్రాంతం అయాన్ల ప్రభావం కారణంగా ద్రావకం యొక్క నిర్మాణంలో గణనీయమైన మార్పుతో వర్గీకరించబడుతుంది.ఇంకా ఎక్కువ సాంద్రత వద్ద, చాలా ద్రావణి అణువులు అయాన్లతో సాల్వేషన్ నిర్మాణాలలో పాల్గొంటాయి, తద్వారా ద్రావకం లోటు ఏర్పడుతుంది.
సాంద్రీకృత ద్రావణం అయానిక్ మెల్ట్ లేదా స్ఫటికాకార సాల్వేట్కు దగ్గరగా ఉండే నిర్మాణాన్ని కలిగి ఉంటుంది, ఇది అయానిక్ నిర్మాణాల యొక్క అధిక క్రమం మరియు ఏకరూపతతో వర్గీకరించబడుతుంది. ఈ అయానిక్ నిర్మాణాలు సంక్లిష్ట పరస్పర చర్యల ద్వారా ఒకదానితో ఒకటి మరియు నీటి అణువులతో బంధిస్తాయి.
వాటి లక్షణాల యొక్క అధిక-ఉష్ణోగ్రత మరియు తక్కువ-ఉష్ణోగ్రత ప్రాంతాలు, అలాగే అధిక మరియు సాధారణ-పీడన ప్రాంతాలు, ఎలక్ట్రోలైట్ల లక్షణం. ఒత్తిడి లేదా ఉష్ణోగ్రత పెరిగేకొద్దీ, ద్రావకం యొక్క మోలార్ క్రమం తగ్గుతుంది మరియు ద్రావణం యొక్క లక్షణాలపై అనుబంధ మరియు సోలేషన్ ప్రభావాల ప్రభావం బలహీనపడుతుంది. మరియు ఉష్ణోగ్రత ద్రవీభవన స్థానం కంటే పడిపోయినప్పుడు, కొన్ని ఎలక్ట్రోలైట్లు గాజు స్థితికి వెళ్తాయి. అటువంటి ఎలక్ట్రోలైట్ యొక్క ఉదాహరణ LiCl యొక్క సజల ద్రావణం.
నేడు, సాంకేతికత మరియు జీవశాస్త్రంలో ఎలక్ట్రోలైట్లు ప్రత్యేకించి ముఖ్యమైన పాత్ర పోషిస్తాయి. జీవ ప్రక్రియలలో, ఎలక్ట్రోలైట్లు అకర్బన మరియు సేంద్రీయ సంశ్లేషణకు మాధ్యమంగా పనిచేస్తాయి మరియు సాంకేతికతలో ఎలెక్ట్రోకెమికల్ ఉత్పత్తికి ఆధారం.
విద్యుద్విశ్లేషణ, ఎలెక్ట్రోక్యాటాలిసిస్, లోహాల తుప్పు, ఎలెక్ట్రోక్రిస్టలైజేషన్ - ఈ దృగ్విషయాలు అనేక ఆధునిక పరిశ్రమలలో, ముఖ్యంగా శక్తి మరియు పర్యావరణ పరిరక్షణ పరంగా ముఖ్యమైన స్థానాలను ఆక్రమించాయి.
ఇది కూడ చూడు: నీటి విద్యుద్విశ్లేషణ ద్వారా హైడ్రోజన్ ఉత్పత్తి - సాంకేతికత మరియు పరికరాలు



