విద్యుద్విశ్లేషణ. గణన ఉదాహరణలు
 విద్యుద్విశ్లేషణ అనేది విద్యుత్ ప్రవాహం ద్వారా ఎలక్ట్రోలైట్ (లవణాలు, ఆమ్లాలు, క్షారాల పరిష్కారం) కుళ్ళిపోవడమే.
విద్యుద్విశ్లేషణ అనేది విద్యుత్ ప్రవాహం ద్వారా ఎలక్ట్రోలైట్ (లవణాలు, ఆమ్లాలు, క్షారాల పరిష్కారం) కుళ్ళిపోవడమే.
విద్యుద్విశ్లేషణ డైరెక్ట్ కరెంట్తో మాత్రమే చేయబడుతుంది. విద్యుద్విశ్లేషణ సమయంలో, ఉప్పులో ఉన్న హైడ్రోజన్ లేదా మెటల్ ప్రతికూల ఎలక్ట్రోడ్ (కాథోడ్) వద్ద విడుదలవుతుంది. సానుకూల ఎలక్ట్రోడ్ (యానోడ్) లోహంతో తయారు చేయబడితే (సాధారణంగా ఉప్పులో అదే), అప్పుడు విద్యుద్విశ్లేషణ సమయంలో సానుకూల ఎలక్ట్రోడ్ కరిగిపోతుంది. యానోడ్ కరగనిది అయితే (ఉదా. కార్బన్), అప్పుడు విద్యుద్విశ్లేషణ సమయంలో ఎలక్ట్రోలైట్ యొక్క మెటల్ కంటెంట్ తగ్గుతుంది.
కాథోడ్ వద్ద విద్యుద్విశ్లేషణ సమయంలో విడుదలయ్యే పదార్ధం మొత్తం ఎలక్ట్రోలైట్ గుండా వెళ్ళిన విద్యుత్ మొత్తానికి అనులోమానుపాతంలో ఉంటుంది.
ఒక కూలంబ్ విద్యుత్ ద్వారా విడుదలయ్యే పదార్ధం మొత్తాన్ని A కి సమానమైన ఎలెక్ట్రోకెమికల్ అంటారు, కాబట్టి G = A • Q; G = A • I • t,
ఇక్కడ G అనేది వివిక్త పదార్ధం యొక్క మొత్తం; Q అనేది విద్యుత్ మొత్తం; I - విద్యుత్ ప్రవాహం; t సమయం.
ప్రతి లోహం దాని ఎలెక్ట్రోకెమికల్ సమానమైన A ని కలిగి ఉంటుంది.
గణన ఉదాహరణలు
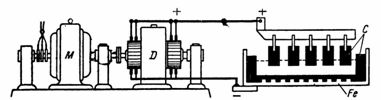
1. 30 నిమిషాల పాటు ప్రస్తుత I = 10 Aతో కాపర్ సల్ఫేట్ (CuSO4) (Fig. 1) నుండి ఎంత రాగి విడుదల చేయబడుతుంది.కాపర్ A = 0.329 mg/Aకి సమానమైన ఎలెక్ట్రోకెమికల్ • సెక.
అన్నం. 1. ఉదాహరణకు పథకం 1
G = A • I • t = 0.329 • 10 • 30 • 60 = 5922 mg = 5.922 g.
కాథోడ్ వద్ద సస్పెండ్ చేయబడిన వస్తువు 5.9 గ్రా స్వచ్ఛమైన రాగిని విడుదల చేస్తుంది.
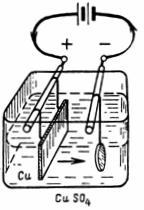
2. రాగి విద్యుద్విశ్లేషణ పూతలో అనుమతించదగిన ప్రస్తుత సాంద్రత • = 0.4 A / dm2. కాథోడ్ యొక్క వైశాల్యం రాగితో కప్పబడి ఉంటుంది S = 2.5 dm2. విద్యుద్విశ్లేషణకు ఏ కరెంట్ అవసరమవుతుంది మరియు 1 గంటలో కాథోడ్ వద్ద ఎంత రాగి విడుదల అవుతుంది (Fig. 2).
అన్నం. 2. ఉదాహరణకు పథకం 2
I = •• S = 0.4-2.5 = l A; G = A • Q = A • I • t = 0.329 • 1 • 60 • 60 = 1184.4 mg.
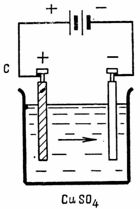
3. విద్యుద్విశ్లేషణ సమయంలో ఆక్సిడైజ్డ్ నీరు (ఉదాహరణకు, సల్ఫ్యూరిక్ ఆమ్లం H2SO4 యొక్క బలహీనమైన పరిష్కారం) హైడ్రోజన్ మరియు ఆక్సిజన్గా కుళ్ళిపోతుంది. ఎలక్ట్రోడ్లు కార్బన్, టిన్, రాగి మొదలైనవి కావచ్చు, కానీ ప్లాటినం ఉత్తమమైనది. యానోడ్ వద్ద ఎంత ఆక్సిజన్ విడుదల అవుతుంది మరియు 1.5 A కరెంట్ వద్ద 1/4 గంటలో కాథోడ్ వద్ద ఎంత హైడ్రోజన్ విడుదల అవుతుంది. విద్యుత్ మొత్తం 1 A సెకను 0.058 cm3 ఆక్సిజన్ మరియు 0.116 cm3 హైడ్రోజన్ను విడుదల చేస్తుంది (Fig. . 3).
అన్నం. 3. ఉదాహరణకు పథకం 3
Ga = A • I • t = 0.058 • 1.5 • 15 • 60 = 78.3 cm3 ఆక్సిజన్ కాథోడ్ వద్ద విడుదల అవుతుంది.
Gc = A • I • t = 0.1162 • 1.5 • 15 • 60 = 156.8 cm3 హైడ్రోజన్ యానోడ్ వద్ద విడుదల చేయబడుతుంది.
ఈ నిష్పత్తిలో హైడ్రోజన్ మరియు ఆక్సిజన్ మిశ్రమాన్ని పేలుడు వాయువు అని పిలుస్తారు, ఇది మండించినప్పుడు పేలుతుంది, నీటిని ఏర్పరుస్తుంది.
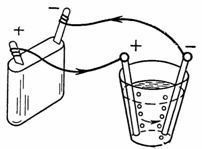
4. ప్రయోగశాల ప్రయోగాలకు ఆక్సిజన్ మరియు హైడ్రోజన్ ఉపయోగించి పొందబడతాయి నీటి విద్యుద్విశ్లేషణ (ఆక్సిడైజ్డ్ సల్ఫ్యూరిక్ యాసిడ్) (Fig. 4). ప్లాటినం ఎలక్ట్రోడ్లు గాజులో కరిగించబడతాయి. ప్రతిఘటనను ఉపయోగించి, మేము ప్రస్తుత I = 0.5 A. (1.9 V యొక్క మూడు పొడి కణాల బ్యాటరీ ప్రస్తుత మూలంగా ఉపయోగించబడుతుంది) 30 నిమిషాల తర్వాత ఎంత హైడ్రోజన్ మరియు ఆక్సిజన్ విడుదల చేయబడుతుంది.
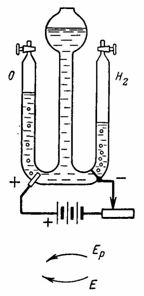
అన్నం. 4… ఉదాహరణకు మూర్తి 4
కుడి పాత్రలో, Gc = A • I • t = 0.1162 • 0.5 • 30 • 60 = 104.58 cm3 హైడ్రోజన్ విడుదల చేయబడుతుంది.
ఎడమ పాత్రలో, Ga = A • l • t = 0.058 • 0.5 • 30 • 60 = 52.2 cm3 ఆక్సిజన్ పరిణామం చెందుతుంది (వాయువులు మధ్య పాత్రలో నీటిని స్థానభ్రంశం చేస్తాయి).
5. కన్వర్టర్ బ్లాక్ (మోటార్-జనరేటర్) విద్యుద్విశ్లేషణ (స్వచ్ఛమైన) రాగిని పొందడం కోసం ప్రస్తుత అందిస్తుంది. 8 గంటల్లో మీరు 20 కిలోల తేనె పొందాలి. జనరేటర్ ఏ కరెంట్ అందించాలి? • రాగికి సమానమైన ఎలెక్ట్రోకెమికల్ A = 0.329 mg/A • సెక.
G = A • I • t, అప్పుడు I = G / (A • t) = 20,000,000 / (0.329 • 8 • 3600) = 20,000,000 / 9475.2 = 2110.7 A.
6. 200 హెడ్లైట్లను క్రోమ్ చేయడం అవసరం, వీటిలో ప్రతిదానికి 3 గ్రా క్రోమ్ అవసరం. ఈ పనిని 10 గంటల్లో చేయడానికి ఎంత కరెంట్ అవసరం (క్రోమియం A = 0.18 mg/A • సెకనుకు సమానమైన ఎలక్ట్రోకెమికల్).
I = G / (A • t) = (200 • 3 • 1000) / (0.18 • 10 • 3600) = 92.6 A.
7. 7 V యొక్క బాత్ మరియు 5000 A కరెంట్ యొక్క వర్కింగ్ వోల్టేజ్ వద్ద స్నానాలలో చైన మట్టి మరియు క్రయోలైట్ యొక్క ద్రావణం యొక్క విద్యుద్విశ్లేషణ ద్వారా అల్యూమినియం పొందబడుతుంది. యానోడ్లు బొగ్గుతో తయారు చేయబడతాయి మరియు స్నానాన్ని బొగ్గుతో ఉక్కుతో తయారు చేస్తారు. బ్లాక్స్ (Fig. 5).
అన్నం. ఉదాహరణకు 5 మూర్తి 5
అల్యూమినియం ఉత్పత్తి స్నానాలు పని వోల్టేజ్ (ఉదాహరణకు, 40 స్నానాలు) పెంచడానికి సిరీస్లో అనుసంధానించబడి ఉంటాయి. 1 కిలోల అల్యూమినియం ఉత్పత్తి చేయడానికి, సుమారు 0.7 కిలోల కార్బన్ యానోడ్లు మరియు 25-30 kWh విద్యుత్ అవసరం. ఇచ్చిన డేటా ఆధారంగా, జనరేటర్ యొక్క శక్తిని, 10 గంటల ఆపరేషన్ కోసం శక్తి వినియోగం మరియు ఫలితంగా అల్యూమినియం యొక్క బరువును నిర్ణయించండి.
40 స్నానాలలో పని చేస్తున్నప్పుడు జనరేటర్ యొక్క శక్తి P = U • I = 40 • 7 • 5000 = 1400000 W = 1400 kW.
10 గంటలపాటు వినియోగించబడే విద్యుత్ శక్తి, A = P • t = 1400 kW 10 h = 14000 kW • h.
పొందిన అల్యూమినియం మొత్తం G = 14000:25 = 560 kg.
సైద్ధాంతిక ఎలక్ట్రోకెమికల్ సమానమైన ఆధారంగా, పొందిన అల్యూమినియం మొత్తం దీనికి సమానంగా ఉండాలి:
GT = A • I • t = 0.093 • 5000 • 40 • 10 • 3600 = 0.093 • 720,000,000 mg = 669.6 kg.
విద్యుద్విశ్లేషణ సంస్థాపన యొక్క సామర్థ్యం దీనికి సమానంగా ఉంటుంది: సమర్థత = G / GT = 560 / 669.6 = 0.83 = 83%.